Phương trình phản ứng
SO2 + KMnO4 + H2O → MnSO4 + K2SO4 + H2SO4 được Cao đẳng nghề Việt Mỹ biên soạn hướng dẫn các bạn học sinh viết và cân bằng đúng phương trình phản ứng khi cho SO2 tác dụng với dung dịch KMnO4.
Phương trình hóa học:
5SO2 + 2KMnO4 + 2H2O → 2MnSO4 + K2SO4 + 2H2SO4
Điều kiện để phản ứng SO2 và KMnO4 xảy ra
Dung môi: H2SO4 loãng.
Cân bằng phản ứng SO2 + KMnO4 + H2O bằng thăng bằng electron
Để cân bằng phương trình phản ứng SO2 và KMnO4 bằng thăng bằng electron, ta phải xác định sự thay đổi số oxi hóa của các chất trong phản ứng:
S+4O2 + KMn+7O4 + H2O → Mn+2SO4 + K2S+6O4 + H2S+6O4
Quá trình oxi hóa: 5x
Quá trình khử: 2x
Phản ứng:
S+4 → S+6 + 2e
Mn+7 +5e → Mn+2
Đặt hệ số cân bằng, ta được phương trình phản ứng:
5SO2 + 2KMnO4 + 2H2O → 2MnSO4 + K2SO4 + 2H2SO4
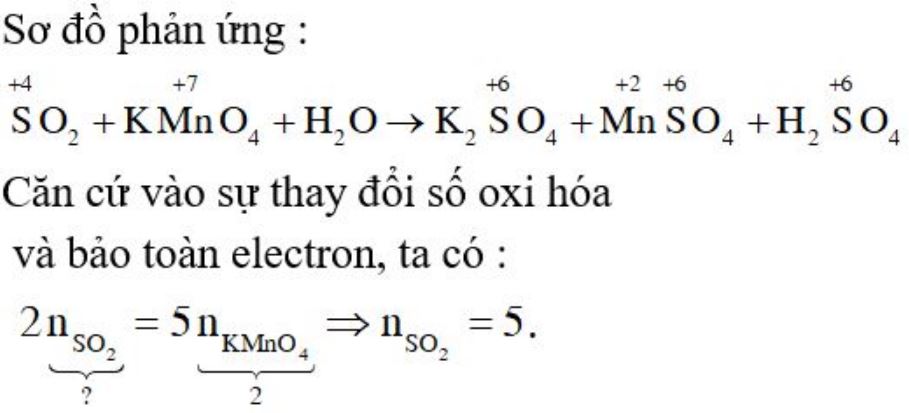
Bài tập vận dụng liên quan
Câu 1. Phương pháp nào sau đây dùng để điều chế khí sunfuro trong phòng thí nghiệm?
A. Đốt lưu huỳnh trong không khí
B. Cho dung dịch K2SO3 tác dụng với H2SO4 đặc
C. Cho tinh thể K2SO3 tác dụng với H2SO4 đặc
D. Đốt cháy khí H2S trong không khí
Đáp án: C
Giải thích:
Trong phòng thí nghiệm, khí sunfuro (SO2) được điều chế bằng cách cho tinh thể K2SO3 tác dụng với H2SO4 đặc.
Việc tạo ra khí sunfuro là cần thiết trong các phản ứng hóa học và sản xuất nhiều chất hoá học như sulfuri, sulfuric acid và sulfat.
Câu 2: Xác định nồng độ dung dịch Br2
Đề bài yêu cầu xác định nồng độ của dung dịch Br2.
Phương trình phản ứng giữa SO2 và KMnO4 là:
5SO2 + 2KMnO4 + 2H2O → 2MnSO4 + K2SO4 + 2H2SO4
Theo đề bài, ta cho SO2 tác dụng với dung dịch Br2:
SO2 + Br2 → HBr + SOBr2
Chú ý rằng phản ứng chỉ diễn ra trong dung dịch, vì SOBr2 rất dễ bay hơi.
Ta thấy rằng khi cho SO2 tác dụng với Br2, Br2 sẽ bị hao hụt và nồng độ Br2 giảm. Do đó, để xác định nồng độ của dung dịch Br2, ta sẽ cho một lượng SO2 cố định vào một lượng dung dịch Br2 cũng cố định và quan sát lượng Br2 còn lại sau phản ứng.
Để thu được lượng Br2 cố định, ta cho 500ml dung dịch Br2 vào bình nước và thổi khí SO2 vào bình cho đến khi mất màu hoàn toàn. Sau đó, ta cho dung dịch NaOH vào bình để trung hòa dung dịch và định mức nồng độ của dung dịch NaOH.
Phương trình phản ứng giữa NaOH và HBr là:
NaOH + HBr → NaBr + H2O
Vì phương trình này có tỉ lệ 1:1 giữa NaOH và HBr, ta sử dụng công thức tính nồng độ như sau:
C(NaOH) × V(NaOH) = C(HBr) × V(HBr)
Từ đó suy ra:
C(HBr) = C(NaOH) × V(NaOH) ÷ V(HBr)
Trong đó:
- C(NaOH) là nồng độ của dung dịch NaOH, đã biết (0,2M)
- V(NaOH) là thể tích dung dịch NaOH đã dùng, đã biết (250ml)
- V(HBr) là thể tích dung dịch HBr, cần tính
Để tính được V(HBr), ta cần biết nồng độ ban đầu của dung dịch Br2. Theo đề bài, dung dịch Br2 có nồng độ là một trong các giá trị sau: 0,025M, 0,01M, 0,02M,
Tham khảo:







































