Polymeđi
Polymeđi là một loại polymer được tạo thành từ việc liên kết các đơn vị monomeđi CH2=CH2 lại với nhau thông qua phản ứng cộng trực tiếp. Công thức đơn giản nhất của polymeđi là (-CH2-CH2-)n, trong đó “n” là số lượng đơn vị monomeđi được liên kết với nhau để tạo thành một chuỗi dài.
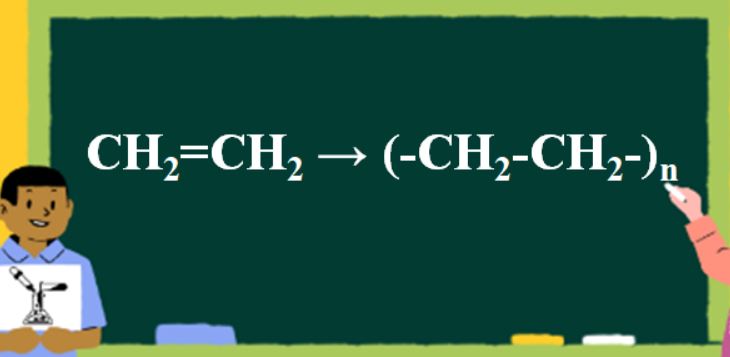
Điều chế polymeđi từ C2H4
Có nhiều phương pháp điều chế polymeđi, bao gồm phương pháp phản ứng trực tiếp, phương pháp chuyển hóa cation và phương pháp chuyển hóa anion.
Phương trình phản ứng
Phản ứng điều chế nhựa Polietylen từ C2H4 được biểu diễn bởi phương trình sau:
nCH2=CH2 → (-CH2-CH2-)n
Trong đó, n là số lượng đơn vị lặp lại của mạch Polietylen và (-CH2-CH2-)n là công thức cấu tạo của Polietylen. Nhựa Polietylen được hình thành từ sự trùng hợp các phân tử eten (C2H4).
Điều kiện điều chế
Phản ứng trùng hợp để tạo ra nhựa Polietylen yêu cầu các điều kiện sau:
- Nhiệt độ cao
- Áp suất cao
- Xúc tác thích hợp
Phản ứng trực tiếp
Phương pháp phản ứng trực tiếp là phương pháp điều chế polymeđi bằng cách tạo ra phản ứng cộng trực tiếp giữa hai đơn vị monomeđi. Phản ứng này được thực hiện bằng cách sử dụng các chất xúc tác như peroxit, ozon hoặc xạ gamma.
Chuyển hóa cation
Phương pháp chuyển hóa cation là phương pháp điều chế polymeđi bằng cách tạo ra cation từ các đơn vị monomeđi và sau đó liên kết chúng lại với nhau. Các chất xúc tác như axit sulfonic, chất khử và chất oxy hóa thường được sử dụng để tạo ra cation.
Chuyển hóa anion
Phương pháp chuyển hóa anion là phương pháp điều chế polymeđi bằng cách tạo ra anion từ các đơn vị monomeđi và sau đó liên kết chúng lại với nhau. Các chất xúc tác như kali hydroxit và chất độn như tetrahydrofuran (THF) thường được sử dụng để tạo ra anion.
Phương trình phản ứng điều chế nhựa PE từ C2H4
Nhựa polietilen (PE)
PE hay còn gọi là polietilen (−CH2−CH2−)n là một loại nhựa tổng hợp được tạo thành từ phản ứng trùng hợp của etylen (C2H4). Khi phản ứng này xảy ra, các phân tử etylen kết hợp lại với nhau thành phân tử có mạch rất dài và phân tử khối lớn là polietilen (PE). Công thức chung của PE là (-CH2-CH2-)n.
Điều kiện điều chế nhựa PE từ C2H4
Để điều chế thành công nhựa PE từ C2H4, cần sử dụng các điều kiện như nhiệt độ cao, áp suất cao và xúc tác thích hợp.
Cách thực hiện phản ứng điều chế nhựa PE từ C2H4
Khi tiến hành phản ứng, các phân tử C2H4 sẽ kết hợp với nhau trong điều kiện nhiệt độ cao, áp suất cao và xúc tác thích hợp để tạo thành phân tử polietilen với mạch rất dài và phân tử khối lớn.
Hiện tượng nhận biết phản ứng C2H4 ra PE
Sản phẩm thu được khi phản ứng C2H4 ra PE là một loại nhựa có mạch rất dài và phân tử khối lớn.
Kiến thức mở rộng
Phản ứng trùng hợp để điều chế nhựa PE từ C2H4 là một trong những phản ứng trùng hợp quan trọng nhất trong ngành hóa học và đồng thời cũng là một trong những phản ứng trùng hợp được ứng dụng rộng rãi nhất trong sản xuất các loại nhựa tổng hợp khác.
Các đồng đẳng của etylen cũng có thể tham gia phản ứng trùng hợp tạo thành các loại nhựa khác như PVC, PS,…
Các bài tập liên quan
Bài 1: Tiến hành trùng hợp 26 gam stiren, hỗn hợp sau phản ứng tác dụng với 500 ml dung dịch Br2 0,15M, cho tiếp dung dịch KI dư vào thu được 3,175 gam Iot. Khối lượng polime tạo ra là: Đáp á
Phương trình phản ứng điều chế axetilen từ metan
Giới thiệu về phản ứng
Phản ứng điều chế axetilen từ metan là một phản ứng quan trọng trong hóa học. Trong phản ứng này, CH4 được phân hủy để tạo ra C2H2 (axetilen) và H2 (hydro). Phản ứng này được sử dụng rộng rãi để sản xuất axetilen, một hợp chất hữu cơ được sử dụng để sản xuất cao su và nhựa, chất oxy hóa và dùng trong công nghiệp hàn.
Công thức phản ứng
Phương trình phản ứng điều chế axetilen từ metan được viết như sau:
CH4 → C2H2 + 2H2
Cơ chế phản ứng
Phản ứng điều chế axetilen từ metan diễn ra ở nhiệt độ cao và trong môi trường không khí. Khi nhiệt độ tăng lên, phân tử CH4 bị phân hủy để tạo ra radican CH3 và H. Radican CH3 tiếp tục phân hủy để tạo ra radican CH2 và H. Radican CH2 tương tác với một phân tử CH4 để tạo ra C2H5 và H. C2H5 sau đó tương tác với một phân tử CH4 khác để tạo ra C2H6. Phân tử C2H6 tiếp tục phân hủy để tạo ra C2H4 và H. Cuối cùng, C2H4 tương tác với một phân tử CH4 khác để tạo ra C2H2 và H2.
Ứng dụng trong công nghiệp
Axetilen được sử dụng rộng rãi trong các ngành công nghiệp như sản xuất cao su và nhựa, sản xuất chất oxy hóa, trong hàn kim loại và trong sản xuất cồn etylic.
Một số bài tập liên quan
Bài tập 1
Tiến hành trùng hợp 26 gam stiren, hỗn hợp sau phản ứng tác dụng với 500 ml dung dịch Br2 0,15M, cho tiếp dung dịch KI dư vào thu được 3,175 gam Iot. Tìm khối lượng polime tạo ra.
Để giải bài tập này, ta cần biết công thức trùng hợp của stiren và phương trình phản ứng giữa Br2 và stiren. Sau đó, ta có thể sử dụng phương trình phản ứng để tính số mol Br2 cần dùng để phản ứng với stiren đã cho. Dựa vào số mol Br2, ta có thể tính số mol polime tạo ra và sử dụng khối lượng mol và khối lượng mol của polime để tính khối lượng polime tạo ra.
Công thức trùng hợp của stiren là:
CH2=CH-Phenyl (Stiren)
Phương trình phản ứng giữa Br2 và stiren là:
C6H5CH=CH2 + Br2 → C6H5CHBrCHBrC6H5
Bước 1: Tính số mol Br2 cần dùng để phản ứng với stiren đã cho.
Số mol Br2 = n = C × V = 0,15 × 0,5 = 0,075 mol
Bước 2: Tính số mol polime tạo ra.
Theo phương trình phản ứng, ta thấy rằng một mol stiren phản ứng với một mol Br2 để tạo ra một mol polime.
Vậy, số mol polime tạo ra là số mol Br2 đã dùng, tức là:
n(polime) = 0,075 mol
Bước 3: Tính khối lượng polime tạo ra.
Khối lượng mol của polime là:
M = m/n = 26 g / 0,075 mol = 346,67 g/mol
Khối lượng polime tạo ra là:
m(polime) = n(polime) × M = 0,075 mol × 346,67 g/mol = 26,000 g
Bước 4: Kiểm tra đáp án.
3,175 g Iot tương đương với số mol Iot là:
n(I) = m/M(I) = 3,175 g / 126,904 g/mol = 0,025 mol
Mỗi mol I2 tương ứng với một mol Br2, do đó số mol Br2 dư là:
n(Br2) = 0,025 mol
Vậy số mol Br2 đã phản ứng là:
n(Br2) = 0,075 – 0,025 = 0,050 mol
Sau đó, ta sử dụng phương trình phản ứng để tính khối lượng polime tạo ra:
n(polime) = n(Br2) = 0,050 mol
m(polime) = n(polime) × M = 0,050 mol × 346,67 g/mol = 17,34 g
Nguồn tham khảo: https://en.wikipedia.org/wiki/Polyethylene






































