Phản ứng hóa học KMnO4 + HCl: Cách thực hiện và ứng dụng trong đời sống
1. Cách thực hiện phản ứng hóa học KMnO4 + HCl
Phản ứng hóa học giữa KMnO4 và HCl là một trong những phản ứng hóa học quan trọng được sử dụng trong nhiều lĩnh vực. Để thực hiện phản ứng này, bạn cần chuẩn bị các vật liệu sau:

- KMnO4 (permanganat kali)
- HCl (axit clohidric)
- Nước
Cách thực hiện phản ứng:
- Cho KMnO4 vào nước và khuấy đều cho tan hoàn toàn.
- Thêm từ từ dung dịch HCl vào dung dịch KMnO4, khuấy đều.
- Quan sát sẽ thấy xuất hiện các khí màu vàng nhạt, màu nâu đỏ và mùi hắc.
- Phản ứng xảy ra theo công thức hóa học:
KMnO4 + HCl → KCl + MnCl2 + Cl2 + H2O
2. Ứng dụng của phản ứng hóa học KMnO4 + HCl trong đời sống
Phản ứng hóa học giữa KMnO4 và HCl được sử dụng trong nhiều lĩnh vực khác nhau, bao gồm:

Tẩy trắng và khử mùi
Phản ứng này được sử dụng để tẩy trắng và khử mùi trong các sản phẩm dệt may và giấy, cũng như trong sản xuất chất tẩy rửa.
Xử lý nước thải
Phản ứng KMnO4 và HCl cũng được sử dụng để xử lý nước thải, giúp loại bỏ các chất độc hại và làm sạch nước thải trước khi đưa vào môi trường.
Sản xuất chất oxy hoá mạnh
KMnO4 và HCl cũng được sử dụng để sản xuất các chất oxy hoá mạnh như manganat kali (K2MnO4) và oxit mangan (MnO2), được sử dụng trong sản xuất pin và pin lithium-ion.
Tổng kết lại, phản ứng hóa học giữa KMnO4 và HCl có nhiều ứng dụng quan trọng trong đời sống và công nghiệp, và việc hiểu rõ cách thực hiện phản ứng này sẽ giúp cho việc áp dụng trong các lĩnh vực này trở nên dễ dàng hơn. Tuy nhiên, cần lưu ý rằng phản ứng này là phản ứng oxi-hoá khử, do đó cần thực hiện trong điều kiện an toàn và đúng cách để tránh các tác động tiêu cực đến sức khỏe và môi trường.
Ngoài ra, cần phải lưu ý rằng phản ứng này là phản ứng exothermic, có thể gây ra nhiệt độ cao, đốt cháy hoặc nổ nếu thực hiện không đúng cách. Vì vậy, khi thực hiện phản ứng, cần phải đeo kính bảo hộ, áo khoác dài và găng tay để bảo vệ cơ thể khỏi các tác động tiêu cực.
Trong việc sử dụng phản ứng KMnO4 và HCl trong các ứng dụng khác nhau, cần phải tuân thủ các quy định và hướng dẫn an toàn của từng lĩnh vực để đảm bảo sự an toàn và hiệu quả trong quá trình sử dụng.
Như vậy, phản ứng hóa học KMnO4 và HCl là một phản ứng quan trọng, có nhiều ứng dụng trong đời sống và công nghiệp. Việc hiểu rõ cách thực hiện phản ứng và các biện pháp an toàn cần thiết trong quá trình sử dụng sẽ giúp cho việc áp dụng của phản ứng này trở nên hiệu quả và an toàn hơn.
Đối với một số ứng dụng cụ thể, phản ứng KMnO4 và HCl được sử dụng như sau:
Làm sạch ống cống và xử lý nước thải: Phản ứng KMnO4 và HCl được sử dụng để làm sạch ống cống và xử lý nước thải. Trong quá trình này, KMnO4 được sử dụng để oxi hóa các chất hữu cơ có trong nước thải, trong khi HCl được sử dụng để điều chỉnh pH của dung dịch.
Xác định nồng độ hỗn hợp HCl và Cl2: Phản ứng KMnO4 và HCl được sử dụng để xác định nồng độ hỗn hợp HCl và Cl2. Trong quá trình này, KMnO4 được sử dụng để oxi hóa HCl thành Cl2, sau đó nồng độ của Cl2 được xác định bằng cách sử dụng các phương pháp phân tích hóa học.
Sản xuất mangan clorua: Phản ứng KMnO4 và HCl được sử dụng để sản xuất mangan clorua. Trong quá trình này, KMnO4 được sử dụng để oxi hóa mangan oxit thành mangan dioxide, sau đó HCl được sử dụng để hòa tan mangan dioxide và tạo ra mangan clorua.
Xử lý sắt và thép: Phản ứng KMnO4 và HCl được sử dụng để xử lý sắt và thép. Trong quá trình này, KMnO4 được sử dụng để loại bỏ các chất gỉ từ sắt và thép, trong khi HCl được sử dụng để loại bỏ các tạp chất có trong sắt và thép.
Trên đây là một số ứng dụng phổ biến của phản ứng hóa học KMnO4 và HCl trong đời sống và công nghiệp. Tuy nhiên, việc sử dụng phản ứng này cần phải tuân thủ các quy định và hướng dẫn an toàn của từng lĩnh vực để đảm bảo sự an toàn và hiệu quả trong quá trình sử dụng.
Bài tập vận dụng liên quan
Câu 1:
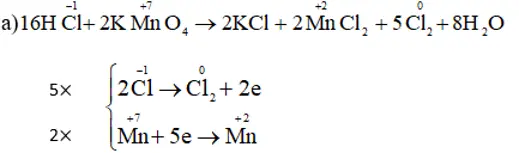
Trong phòng thí nghiệm, người ta điều chế oxi bằng cách nhiệt phân KClO3 hoặc KMnO4 hoặc KNO3 vì chúng giàu oxi và dễ phân hủy ra oxi.
Câu 2:
Trong phòng thí nghiệm cần điều chế 4,48 lít O2 (Đktc). Chất có khối lượng nhỏ nhất cần dùng là KClO3.
Câu 3:
Cho 14,6 gam HCl tác dụng hết với KMnO4, thu được V lít khí Cl2 (đktc). Giá trị của V là 2,8 lít.
Câu 4:
Trong phòng thí nghiệm, người ta thường điều chế clo bằng cách cho dung dịch HCl đặc tác dụng với MnO2, đun nóng.
Câu 5:
Chất dùng để làm khô khí Cl2 ẩm là CaO.
Câu 6:
Đặc điểm chung của các đơn chất halogen (F2, Cl2, Br2, I2) là tính chất hóa học cơ bản là tính oxi hóa.
Câu 7:
Cho clo vào nước, thu được nước clo gồm H2O, HCl, HClO và Cl2.
Câu 8:
Dãy gồm các chất đều tác dụng được với dung dịch HCl loãng là KHCO3, AgNO3 và CuO.
Câu 9:
Trong số các chất KMnO4, KClO3, KNO3, H2O2, chất nào khi nhiệt phân cùng một lượng số mol thu được lượng khí oxi lớn nhất là KClO3.
Đề thi hóa học
Câu 1
Cho các chất sau: KMnO4, KClO3, KNO3, H2O2. Chất nào tạo ra lượng khí O2 lớn nhất khi nhiệt phân 1 mol của chất đó?
Đáp án: B
Giải thích: Theo phương trình hóa học nhiệt phân của từng chất, ta tính được số mol khí O2 tạo ra. Với chất KClO3 thì tạo ra số mol O2 lớn nhất.
Câu 10
Cho KMnO4 tác dụng với HCl đặc thu được khí A. Dẫn khí thu được vào dung dịch KOH ở nhiệt độ thường và đun nóng. Cho biết hiện tượng xảy ra.
Đáp án: A
Giải thích: KMnO4 tan trong HCl làm mất màu dung dịch thuốc tím và tạo ra khí màu vàng lục (Cl2). Tiếp tục cho khí Cl2 vào dung dịch KOH thì tạo ra dung dịch không màu và khí thoát ra.
giải thích sản phẩm phản ứng KMnO4 + HCl – YouTube
Bạn Đang Xem Bài Viết: Phản ứng hóa học KMnO4 + HCl Cách thực hiện và ứng dụng trong đời sống







































