Phản ứng giữa Cl2 và NaOH
Phương trình phản ứng: Cl2 + 2NaOH → NaCl + NaClO + H2O Nước giaven được tạo thành trong quá trình này.
Điều kiện phản ứng Clo tác dụng với NaOH
Điện phân dung dịch NaCl có màng ngăn bằng xốp với điện cực dương bằng than chì và điện cực âm làm bằng sắt.
Vậy phản ứng được thực hiện trong điều kiện điện phân.
Hiện tượng khi Clo tác dụng với NaOH
Dẫn khí Clo vào dung dịch NaOH loãng, giấy quỳ tím sẽ bị mất màu. Sản phẩm thu được là nước Giaven.
Khái niệm và đặc tính của nước Giaven
Nước Giaven (hay còn gọi là nước Javen) là một hỗn hợp được tạo thành từ hai muối NaCl và NaClO khi sục khí Clo dư vào Natri Hydroxit.
Nước Giaven có tính oxy hóa mạnh, được sử dụng làm chất tẩy rửa cực mạnh. Thành phần chính của nước Giaven là NaClO, một axit có tính oxi hóa rất mạnh.
Chất Cl và ứng dụng trong điều chế nước Javen
Trong hợp chất, Cl có số oxi hóa +1, do vậy nó có khả năng oxi hóa mạnh các chất để trở về số oxi hóa thấp hơn. Các hợp chất phức hữu cơ dưới dạng các vết mực, vết màu dính trên quần áo, vật liệu sẽ bị tính oxi hóa mạnh của phân tử NaClO làm phá vỡ nên sẽ nhanh chóng tẩy được những vết bẩn rất hữu hiệu. Nước Javen là hỗn hợp có mùi xốc khi sử dụng.
Trong môi trường axit, NaClO phản ứng theo phương trình:
NaClO + 2HCl → NaCl + Cl2 + H2O
Khí Cl2 tạo thành có mùi xốc, khi ảnh hưởng xấu đến sức khỏe con người khi hít phải. Nên chúng ta phải cẩn thận khi sử dụng hóa chất này.
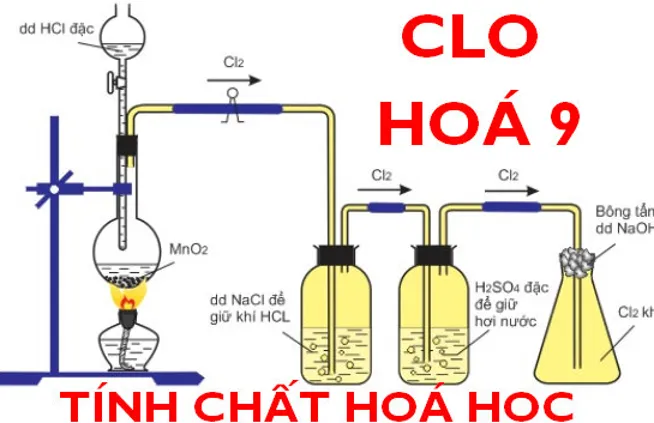
Điều chế nước javen trong phòng thí nghiệm
Cách 1: Điều chế từ Cl2 và NaOH
Trong phòng thí nghiệm, nước javen được điều chế trực tiếp bằng Cl2 và dung dịch NaOH. Chúng ta tiến hành cho khí Cl2 đi qua dung dịch NaOH ở nhiệt độ thường. Kết quả của phản ứng sẽ tạo ra hỗn hợp dung dịch NaCl và nước giaven. Phương trình phản ứng như sau:
Cl2 + 2NaOH → NaCl + NaClO + H2O
Cách 2: Điều chế từ MnO2 và HCl
Ở phương pháp này, người ta sẽ tiến hành cho hóa chất MnO2 phản ứng với axit HCl để tạo ra khí clo. Sau đó tiếp tục sục khí Cl2 đi qua dung dịch NaOH sẽ thu được hóa chất NaClO (nước gia-ven). Phương trình phản ứng:
4HCl + MnO2 → Cl2
Phương trình phản ứng hóa học Cl2 + NaOH → NaCl + NaClO + H2O
Trong đó:
- Cl2: khí clo
- NaOH: dung dịch hidroxit natri
- NaCl: muối cloua
- NaClO: cloua natri
- H2O: nước
Các đáp án:
- Khí clo có màu vàng lục, mùi sốc, tan ít trong nước, rất độc.
- Khí clo không màu, mùi sốc, tan ít trong nước, rất độc.
- Khí clo có màu vàng lục, mùi sốc, tan ít trong nước, rất độc.
- Màu vàng lục, mùi hắc, tan nhiều trong nước, rất độc.
Đáp án cho câu hỏi “Trong công nghiệp, khí clo có thể được sản xuất bằng cách nào sau đây?” là A, tức là “điện phân dung dịch NaCl có màng ngăn xốp”.
Câu hỏi liên quan đến Clo
Câu 1:
Nước Gia-ven là hỗn hợp các chất nào sau đây?
A. HCl, HClO, H2O
B. NaCl, NaClO4, H2O
C. NaCl, NaClO, H2O
D. NaCl, NaClO3, H2O
Đáp án: C
Câu 2:
Vì sao nước clo có tính tẩy màu?
A. vì khi dẫn khí clo vào nước không xảy ra phản ứng hoá học
B. Vì clo tác dụng với nước tạo nên axit HCl có tính tẩy màu
C. Vì clo hấp phụ được màu
D. Vì clo tác dụng nước tạo nên axit HClO có tính tẩy màu
Đáp án: D: Vì clo tác dụng nước tạo nên axit HClO có tính tẩy màu
Câu 3:
Thành phần của nước clo có chứa những chất nào dưới đây?
A. H2O, Cl2, HClO3
B. HCl, HClO
C. Cl2, HCl, HClO2
D. Cl2, HCl, HClO
Đáp án: D
Câu 4:
Thực hiện thí nghiệm cho Cl2 tác dụng với dung dịch NaOH ở nhiệt độ thường, trong phản ứng dưới đây Cl2 đóng vai trò là:
2NaOH + Cl2 → NaCl + NaClO + H2O
A. chất nhường proton.
B. chất nhận proton.
C. chất nhường electron cho NaOH.
D. vừa là chất khử, vừa là chất oxi hóa.
Đáp án: D
Câu 5:
Trong tự nhiên, clo tồn tại chủ yếu ở dạng nào?
A. muối clorua
B. muối natri clorat
C. Axit clohidric
D. Đơn chất
Đáp án: A
Nguồn tham khảo: https://vi.wikipedia.org/wiki/Chlor







































