Công thức tính nồng độ phần trăm và bài tập vận dụng
Định nghĩa về nồng độ phần trăm
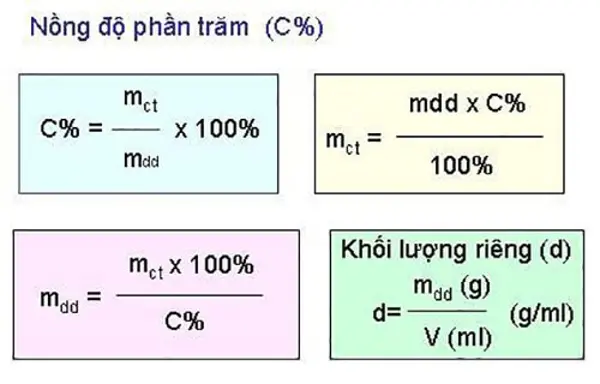
Trong môn hóa học, nồng độ phần trăm (C%) là đại lượng cho biết số gam chất tan có trong 100 gam dung dịch. Để hiểu rõ hơn về nồng độ phần trăm, ta sử dụng công thức sau đây:

C% = (mct/mdd) x 100%
Trong đó:
C% là ký hiệu của nồng độ phần trăm
mct là ký hiệu của khối lượng chất tan
mdd là ký hiệu của khối lượng dung dịch
Ta có công thức để xác định khối lượng dung dịch như sau:
(mdd = mdm + mct)
Trong đó, mdm là khối lượng của dung môi.
Các bước cơ bản để giải bài toán tính nồng độ phần trăm
Để giải một bài toán về nồng độ phần trăm, ta có các bước sau:
Bước 1: Xác định số chất có trong dung dịch, đặc biệt là các số dư của chất tham gia phản ứng. Việc xác định sai số dư có thể làm cho kết quả sai lệch rất nhiều. Đây là hướng mà một số bài toán trắc nghiệm thường khai thác.
Bước 2: Tính khối lượng dung dịch sau khi tham gia phản ứng theo phương pháp bảo toàn khối lượng (tổng khối lượng chất tham gia = tổng khối lượng chất sản phẩm). Bước thứ 2 này trở nên đơn giản hơn nhờ ĐLBTKL.
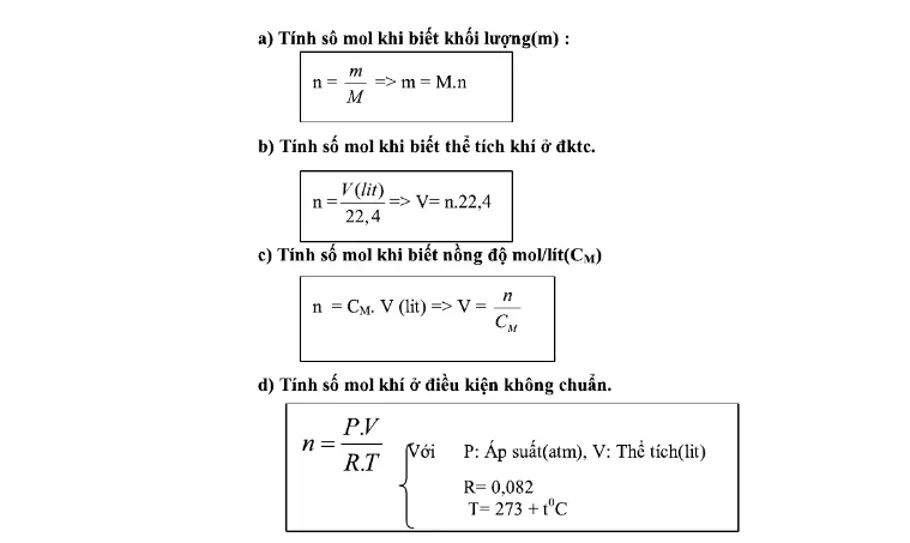
Bước 3: Tính khối lượng chất tan bằng công thức: m = M x n.
Bước 4: Áp dụng công thức tính nồng độ phần trăm để giải bài toán.
Ngoài ra, còn có những bài tập không cho trước khối lượng của chất cần tính, khi đó ta cần áp dụng các kiến thức đã học kết hợp với công thức để giải bài toán. Việc một số bài toán không cho trước khối lượng nhưng có một vài phương pháp bảo toàn giúp ta tính toán khá nhanh. Nắm vững công thức tính nồng độ phần trăm sẽ giúp các em giải được nhiều bài toán khác nhau trong môn hóa học.
Bài tập tự luận về nồng độ phần trăm
Bài 1: Tính nồng độ phần trăm của dung dịch đường
Hãy tính nồng độ phần trăm của dung dịch thu được khi hòa tan 10 gam đường vào 40 gam nước.
Khối lượng của dung dịch là:
Ta có: mdd = mdm + mct = 10 + 40 = 50 gam (mdm là khối lượng dung môi)
Nồng độ phần trăm: C% = (mct/mdd) * 100% = (10/50) * 100% = 20%
Vậy nồng độ phần trăm của dung dịch thu được sau phản ứng là 20%.
Bài 2: Tính khối lượng NaOH trong dung dịch
Hãy tính khối lượng NaOH có trong 200 gam dung dịch chất NaOH 15%
Ta có: mNaOH = (C% * mdd) / 100 = 15 * 200 / 100 = 30 gam.
Vậy nồng độ dung dịch NaOH trong dung dịch là 15%.
Bài 3: Tính khối lượng nước và dung dịch muối
Đem hoà tan 20 gam muối vào nước được dd có nồng độ 10%. Hãy tính:
a)Tính khối lượng dung dịch nước muối thu được
b)Tính khối lượng nước cần dùng cho sự pha chế
a) mdd = (mmuối * 100) / C% = (20 * 100) / 10 = 200 gam
b) m(nước) = mdd – mmuối = 200 – 20 = 180 gam
Đáp số: mdd = 200 gam và mH2O = 180 gam
Bài 4: Tính khối lượng NaOH trong dung dịch
Hãy tính khối lượng của NaOH có trong 200g dung dịch NaOH 15%
Áp dụng công thức tính nồng độ %: C% = (mct/mdd) * 100% ta có:
C% = (mNaOH/200) * 100 = 15 (%) => mNaOH = (15 * 200) / 100 = 30 (g)
Vậy trong 200g dung dịch NaOH 15% có 30 gam NaOH
Bài 5: Tính khối lượng nước và dung d
Bài tập trắc nghiệm
Câu 1. Tính nồng độ phần trăm của dung dịch H2SO4 sau khi phản ứng với 100 gam ?O3 và 500 ml dung dịch H2SO4 17%
A. 35%
B. 34%
C. 33%
D. 32%
Câu 2. Tính khối lượng CuSO4.5H2O cần thêm vào để tạo thành dung dịch CuSO4 34% từ 75 gam dung dịch CuSO4 14% (Bài toán muối ngậm nước)
A. 55 gam
B. 56 gam
C. 57 gam
D. 50 gam
Câu 3. Tính khối lượng nước cần dùng để hòa tan 40 gam KOH để tạo thành dung dịch KOH 32%
A. 50 gam
B. 60 gam
C. 80 gam
D. 85 gam
Câu 4. Trộn 1 lít dung dịch HNO3 10% (D = 1,054 g/ml) với 2 lít dung dịch HNO3 24% (D = 1,14 g/ml). Tính nồng độ phần trăm của dung dịch sau phản ứng:
A. 19,57%
B. 18,4%
C. 17,33%
D. 16,32%
Câu 5. Tính nồng độ mol và phần trăm của dung dịch HCl thu được sau khi hòa tan 36,5 gam HCl vào đủ nước với khối lượng riêng D = 1,1 g/ml
A. 2M và 6,64%
B. 1,5M và 4,5%
C. 3M và 7%
D. 0.75M và 3,5%
Trong các bài toán về hóa học, công thức tính nồng độ phần trăm là rất quan trọng. Việc nắm vững công thức này sẽ giúp bạn giải quyết các bài toán về hóa học một cách dễ dàng hơn. Hãy lưu ý rằng công thức này áp dụng không chỉ trong hóa học vô cơ mà còn cả trong hóa học hữu cơ.
[RẤT DỄ] – HOÁ 9 – TÍNH NỒNG ĐỘ PHẦN TRĂM CÁC CHẤT TRONG DUNG DỊCH SAU PHẢN ỨNG – YouTube
Bạn Đang Xem Bài Viết: Công thức tính nồng độ phần trăm và bài tập vận dụng






































