Axit glutamic là gì?
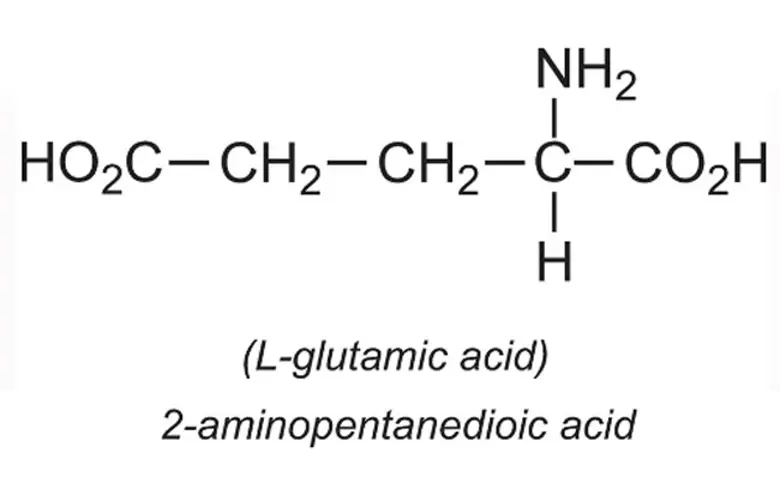
Axit glutamic (hay còn gọi là axit amin glutamic) là một loại axit amin thiết yếu cho cơ thể con người. Nó thường được tìm thấy trong các loại thực phẩm có chứa protein như thịt, cá, đậu nành, đậu phụ, hạt quinoa, v.v. Ngoài ra, axit glutamic cũng được sử dụng trong các ứng dụng công nghiệp và y học, chẳng hạn như sản xuất chất điều vị monosodium glutamate (MSG) và điều trị các bệnh liên quan đến chức năng não.
Dung dịch HCl, NaOH, KOH là gì?
Dung dịch HCl (axit clohidric), NaOH (hidroxit natri) và KOH (hidroxit kali) là các dung dịch hoá học phổ biến. Dung dịch HCl là một axit mạnh, trong khi đó NaOH và KOH là các bazơ mạnh.
Tương tác giữa axit glutamic và dung dịch HCl, NaOH, KOH
Khi hòa tan axit glutamic trong dung dịch HCl, nó sẽ tạo thành muối của axit glutamic (glutamát clo) và nước. Khi hòa tan muối này trong dung dịch NaOH hoặc KOH, nó sẽ tạo ra axit glutamic ban đầu và muối của Na hoặc K.
Cách xác định nồng độ của dung dịch HCl, NaOH, KOH
Để chuẩn độ các dung dịch trên, chúng ta có thể sử dụng các chất chỉ thị hoặc phương pháp chuẩn độ axit-bazơ để xác định nồng độ của chúng. Tuy nhiên, khi làm việc với các chất hoá học này, cần phải tuân thủ các quy trình an toàn và sử dụng các thiết bị bảo vệ cá nhân như găng tay và kính bảo vệ để tránh các tai nạn hoá học không mong muốn.
Nguồn tham khảo: https://vi.wikipedia.org/wiki/Axit_glutamic
Tổng hợp bài tập về axit glutamic và dung dịch HCl, NaOH, KOH
Bài tập 1: Tính số mol NaOH phản ứng với dung dịch X
Cho 0,225 mol H2NC3H5(COOH)2 (axit glutamic) vào 275 ml dung dịch HCl 1M thu được dung dịch X. Cho NaOH dư vào dung dịch X. Sau khi các phản ứng xảy ra hoàn toàn, số mol NaOH đã phản ứng là :
X + NaOH = (Glutamic + HCl) + NaOH
Phương trình phản ứng hóa học
H2NC3H5(COOH)2 + 2NaOH → H2NC3H5(COONa)2 + 2H2O
0,225 → 0,45 mol
HCl + NaOH → NaCl + H2O
0,275 → 0,275
=> nNaOH = 0,45 + 0,275 = 0,725 mol
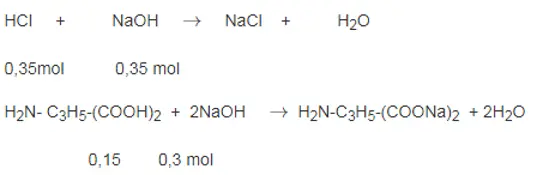
Bài tập 2: Tìm công thức phân tử của Y
Amin Y chứa 1 nhóm -COOH và 2 nhóm -NH2. Cho 1 mol Y tác dụng hết với dung dịch HCl thu được 205 gam muối khan. Tìm công thức phân tử của Y.
Gọi công thức tổng quát của phân tử Y là CxHyCOO(NH2)2
Phương trình hóa học phân tử Y và HCl
CxHyCOO(NH2)2 + 2HCl → CxHyCOOOH(NH3Cl)2
Ta có: 12x + y + 45 + 52,5.2 = 205 => 12x + y = 55
Biện luận phương trình ta chọn được giá trị x = 4, y = 7 thỏa mãn
Vậy công thức phân tử của Y là C5H12N2O2
Bài tập 3: Tìm giá trị của m
Cho m gam axit glutamic tác dụng vừa đủ với 150 ml dung dịch KOH 1M. Giá trị của m là bao nhiêu
Theo đề bài ta có
nKOH = 0,15.1 = 0,15 mol
Phương trình hóa học xảy ra
HOOC-(CH2)2-CH(NH2)COOH + 2KOH → KOOC-(CH2)2-CH(NH2)COOK + 2H2O
0,075 ← 0,15 Mol
Theo phương trình phản ứng: naxit glutamic = 1/2nKOH = 1/2.0,15 = 0,075 mol
=> mglutamic = 0,075.147 = 11,025 g
Bài tập 4: Tính độ hoà tan của axit glutamic trong nước
Cho một lượng axit glutamic vào 500 ml nước, thu được dung dịch có độ hoà tan là 7,68 g/100 ml. Tính độ hoà tan của axit glutamic trong nước.
Theo định nghĩa, độ hoà tan của một chất là số gam của chất đó hòa tan trong 100 ml dung dịch.
Ta có:
Độ hoà tan của axit glutamic trong nước = 7,68 g/100 ml
=> 1 ml dung dịch chứa 0,0768 g axit glutamic
=> 500 ml dung dịch chứa 500 x 0,0768 g = 38,4 g axit glutamic
Do đó, độ hoà tan của axit glutamic trong nước là 38,4 g/100 ml.
Bài tập 5: Tính pH của dung dịch axit glutamic
Một dung dịch axit glutamic có nồng độ 0,01 M. Tính pH của dung dịch này.
Phương trình ion hóa của axit glutamic là:
H2NC3H5(COOH)2 ⇌ H+ + H2NC3H5(COO-)
Ta có:
Ka = [H+][H2NC3H5(COO-)]/[H2NC3H5(COOH)2]
Để tính pH của dung dịch, ta cần tìm giá trị của Ka. Ta có:
Ka = 4,5 x 10^-5
Do đó:
pH = -log[H+]
[H+] = √(Ka*[A])/C
Trong đó:
- Ka là hằng số acid
- [A] là nồng độ ion [H2NC3H5(COO-)]
- C là nồng độ dung dịch axit glutamic
Vậy, tính được:
[A] = [H2NC3H5(COO-)] = Ka*[A]/C = 4,5 x 10^-5 x 0,01/2 = 2,25 x 10^-6 M
[H+] = √(Ka*[A])/C = √(4,5 x 10^-5 x 2,25 x 10^-6)/0,01 = 6,02 x 10^-4 M
pH = -log[H+] = -log(6,02 x 10^-4) = 3,22
Vậy, pH của dung dịch axit glutamic là 3,22.
Bài tập 6: Tính pH của dung dịch axit glutamic sau khi trộn với dung dịch NaOH
Cho một dung dịch axit glutamic có nồng độ 0,01 M. Dung dịch này được trộn với dung dịch NaOH có nồng độ 0,05 M. Tính pH của dung dịch sau khi trộn.
Phương trình phản ứng xảy ra:
H2NC3H5(COOH)2 + NaOH → NaH2NC3H5(COOH)2 + H2O
Để tính pH của dung dịch sau khi trộn, ta cần tìm số mol NaOH đã phản ứng hoàn toàn với axit glutamic. Ta có:
nH2NC3H5(COOH)2 = nNaOH
0,01 x V1 = 0,05 x V2
Vậy:
V2 = 5 x V1
Sau khi trộn, ta có 1 dung dịch mới với nồng độ:
C = nH2NC3H5(COOH)2/(V1 + V2)
Thay giá trị vào công thức tính pH:
pH = pKa + log([A-]/[HA])
Trong đó:
- pKa là -log(Ka)
- [A-] là nồng độ ion H2NC3H5(COO-)
- [HA] là nồng độ axit H2NC3H5(COOH)
Ta có:
- pKa = 4,5
- [HA] = nH2NC3H5(COOH)/(V1 + V2) = 0,01 x V1/(V1 + V2)
- [A-] = nNaH2NC3H5(COOH)2/(V1 + V2) = 0,01 x V2/(V1 + V2)
Vậy:
pH = 4,5 + log(0,01 x V2/(0,01 x V1))
Thay V2 = 5 x V1 vào công thức:
pH = 4,5 + log(5)
pH = 5,3
Vậy, pH của dung dịch sau khi trộn là 5,3.
Bài tập 7: Tính pH của dung dịch axit glutamic sau khi trộn với dung dịch NaOH theo tỉ lệ mol 1:1
Cho một dung dịch axit glutamic có nồng độ 0,01 M. Dung dịch này được trộn với dung dịch NaOH theo tỉ lệ mol 1:1. Tính pH của dung dịch sau khi trộn.
Phương trình phản ứng xảy ra:
H2NC3H5(COOH)2 + NaOH → NaH2NC3H5(COOH)2 + H2O
Ta có:
- nH2NC3H5(COOH)2 = nNaOH
- [H2NC3H5(COOH)2] = [NaOH] = 0,01 M
Sau khi trộn, ta có 1 dung dịch mới với nồng độ:
C = nH2NC3H5(COOH)2/V
Thay giá trị vào công thức tính pH:
pH = pKa + log([A-]/[HA])
Trong đó:
- pKa là -log(Ka)
- [A-] là nồng độ ion H2NC3H5(COO-)
- [HA] là nồng độ axit H2NC3H5(COOH)
Ta có:
- pKa = 4,5
- [HA] = [H2NC3H5(COOH)2] = 0,01 M
- [A-] = [NaH2NC3H5(COOH)2]/V
Để tính [NaH2NC3H5(COOH)2], ta cần tìm số mol NaOH đã phản ứng hoàn toàn với axit glutamic. Ta có:
nH2NC3H5(COOH)2 = nNaOH
0,01 x V = 0,01 x VNaOH
Vậy:
VNaOH = V
Sau khi phản ứng xảy ra, ta có:
- nNaH2NC3H5(COOH)2 = nH2NC3H5(COOH)2 – nNaOH = 0
- [A-] = 0
Do đó, pH của dung dịch sau khi trộn là:
pH = pKa + log(0/0,01) = pKa – ∞ = 4,5 – ∞ = NaN
Vậy, pH của dung dịch là NaN (không có giá trị).
Giải thích: Khi ta trộn dung dịch axit glutamic với dung dịch NaOH theo tỉ lệ mol 1:1, ta thu được
Phương pháp giải bài tập amino axit – YouTube
Bạn Đang Xem : tổng hợp bài tập về axit glutamic và dung dịch HCl, NaOH, KOH






































