Phản ứng NH3 + HNO3 → NH4NO3
Phản ứng giữa amoniac và axit nitric tạo thành muối amoni nitrat (NH4NO3), được biết đến như là phản ứng trung hòa. Trong quá trình phản ứng, nhóm amoni (NH3) đóng vai trò như một bazơ, nhận proton từ axit nitric (HNO3) để tạo ra ion amoni (NH4+) trong khi các ion nitrat (NO3-) được giữ lại. Phản ứng có thể được biểu diễn bằng phương trình hóa học sau:

NH3 + HNO3 → NH4NO3
Phản ứng này là một phản ứng cân bằng và xảy ra trong điều kiện ấm và có mặt của nước.
Phương trình phản ứng HNO3 ra NH4NO3
Phương trình phản ứng HNO3 ra NH4NO3 là: NH3 + HNO3 → NH4NO3. Việc hiểu và sử dụng phương trình phản ứng này một cách chính xác sẽ giúp cho các bạn học tập và giải quyết các dạng bài tập tương tự một cách hiệu quả.
Điều kiện phản ứng NH3 tác dụng HNO3
Khi cho NH3 tác dụng với dung dịch HNO3, điều kiện cần lưu ý là nhiệt độ.
Ứng dụng
Muối amoni nitrat (NH4NO3) được sử dụng rộng rãi trong lĩnh vực nông nghiệp, dược phẩm và công nghiệp nổ. Trong lĩnh vực nông nghiệp, muối amoni nitrat được sử dụng như một loại phân bón để cung cấp nitơ cho cây trồng. Trong dược phẩm, nó được sử dụng để sản xuất một số loại thuốc. Ngoài ra, muối amoni nitrat cũng được sử dụng trong công nghiệp nổ để sản xuất thuốc nổ, tấm chắn, và các sản phẩm khác. Tuy nhiên, việc sử dụng muối amoni nitrat cần được thực hiện cẩn thận vì nó có thể gây ra nguy hiểm nếu bị cháy hoặc nổ.
Ngoài ra, muối amoni nitrat còn được sử dụng như một chất ức chế sương mù. Nó được phun trực tiếp vào không khí để làm giảm độ ẩm và ngăn chặn sương mù.
Muối amoni nitrat cũng được sử dụng trong sản xuất phân bón hữu cơ. Khi kết hợp với các chất phân hủy hữu cơ, muối amoni nitrat giúp tăng cường sự phân hủy và giải phóng các chất dinh dưỡng trong đất. Điều này giúp cây trồng hấp thụ các chất dinh dưỡng hiệu quả hơn và tăng năng suất.
Tuy nhiên, việc sử dụng muối amoni nitrat cũng có những hạn chế. Nó có thể gây ra ô nhiễm môi trường nếu không được sử dụng đúng cách. Việc sử dụng quá nhiều phân bón chứa muối amoni nitrat có thể dẫn đến sự mất cân bằng dinh dưỡng trong đất và gây ra các vấn đề môi trường khác.
Tóm lại, phản ứng giữa NH3 và HNO3 tạo thành muối amoni nitrat (NH4NO3) được sử dụng rộng rãi trong nông nghiệp, dược phẩm, công nghiệp nổ và như một chất ức chế sương mù. Tuy nhiên, việc sử dụng muối amoni nitrat cần được thực hiện cẩn thận để tránh gây ra hại cho môi trường và con người.
Bài tập vận dụng liên quan
Dưới đây là một số bài tập liên quan đến phản ứng NH3 tác dụng HNO3:
Câu 1. Phản ứng nào sau đây thể hiện tính khử của NH3
Đáp án: C. 3NH3 + 3H2O + AlCl3 → Al(OH)3 + 3NH4Cl.
Câu 2. Chất nào sau đây có thể làm khô khí NH3 có lẫn hơi nước?
Đáp án: B. H2SO4 đặc.
Câu 3. Khi dẫn khí amoniac vào bình chứa clo thì phản ứng tạo ra khói trắng. Hợp chất được tạo thành chính là:
Đáp án: C. NH4Cl.
Câu 4. Hợp chất nào sau đây là thành phần chính của đạm hai lá?
Đáp án: A. NH4NO3.
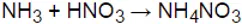
Câu 5. Cho dung dịch NH4NO3 tác dụng với dung dịch bazơ của kim loạithu được 4,48 lít khí (đktc) và 26,1 gam muối. Kim loại đó là
Đáp án: D. Ba.
Câu 6. Phản ứng hóa học nào sau dây chứng tỏ amoniac là một chất khử mạnh?
Đáp án: C. 2NH3 + 3CuO → N2 + 3Cu + 3H2O.
Câu 7. Đốt cháy hổn hợp gồm 6,72 lít khí Oxi và 7 lít khí amoniac (đo ở cùng điều kiện nhiệt độ và áp suất). Sau phản ứng thu được nhóm
Tìm hiểu thêm kiến thức các môn học lớp 11
Để giúp các bạn học sinh lớp 11 có thêm tài liệu và kiến thức để học tập và chuẩn bị cho kì thi học kỳ 1 và học kỳ 2, Cao đẳng nghề Việt Mỹ xin giới thiệu một số tài liệu và đề thi các môn học Toán, Ngữ văn và Tiếng Anh lớp 11.
Tài liệu và đề thi học kỳ 1 lớp 11
Bao gồm các tài liệu và đề thi của các môn học Toán, Ngữ văn và Tiếng Anh lớp 11 để các bạn có thể ôn tập và củng cố kiến thức trước kì thi học kỳ 1.
Tài liệu và đề thi học kỳ 2 lớp 11
Bao gồm các tài liệu và đề thi của các môn học Toán, Ngữ văn và Tiếng Anh lớp 11 để các bạn có thể ôn tập và củng cố kiến thức trước kì thi học kỳ 2.
Bài tập về axit nitric (HNO3) – Hóa học 11- Thầy Phạm Thanh Tùng – YouTube
Bạn Đang Xem Bài Viết: Phản ứng NH3 + HNO3 → NH4NO3 và ứng dụng







































