Phản ứng S + HNO3 là một trong những phản ứng quan trọng trong hóa học vì nó tạo ra hai sản phẩm chính là H2SO4 và NO2. Trong bài viết này, chúng ta sẽ tìm hiểu về cơ chế phản ứng, cách thức thực hiện, và ứng dụng trong sản xuất công nghiệp.

Cơ chế phản ứng S + HNO3
Phản ứng S + HNO3 là một phản ứng oxy hóa khá phức tạp. Cơ chế phản ứng được giải thích như sau:
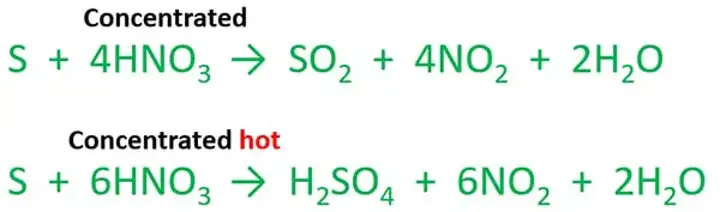
Trong phản ứng này, HNO3 được sử dụng làm chất oxy hóa và S được sử dụng làm chất khử. Khi HNO3 tác dụng với S, HNO3 chuyển electron cho S, giúp S được oxy hóa thành SO2. Trong khi đó, NO2 được giải phóng và H2SO4 được tạo ra như sản phẩm chính của phản ứng. Phản ứng còn tạo ra một lượng nhỏ H2O.
Cách thực hiện phản ứng S + HNO3
Phản ứng S + HNO3 được thực hiện trong một bình kín, có thể chịu được áp suất và nhiệt độ cao. Để tăng tốc độ phản ứng, người ta thường thêm H2SO4 vào bình phản ứng. H2SO4 giúp tăng tính ổn định của phản ứng, tăng cường sự phân hủy của HNO3, và đồng thời giúp phản ứng diễn ra nhanh hơn.
Việc thực hiện phản ứng S + HNO3 cần phải được thực hiện rất cẩn thận, vì phản ứng này có thể tạo ra một số chất độc hại, như NO2 và SO2. Do đó, nếu không được thực hiện đúng cách, phản ứng này có thể gây nguy hiểm cho sức khỏe và môi trường.
Ứng dụng trong sản xuất công nghiệp
Phản ứng S + HNO3 được sử dụng rộng rãi trong sản xuất phân bón và hóa chất công nghiệp. H2SO4 và NO2 được sử dụng để sản xuất axit nitric và các chất hữu cơ. Ngoài ra, phản ứng S + HNO3 còn được sử dụng để sản xuất chất tẩy trắng, chất phụ gia trong sản xuất cao su, giấy và dệt nhuộm. Nó cũng được sử dụng trong các phương pháp phân tích hóa học để phát hiện các ion sulfat, nitrat và nitrit trong mẫu thử.
Trong sản xuất phân bón, H2SO4 được sử dụng để sản xuất axit phosphoric, một thành phần quan trọng trong phân bón. NO2 được sử dụng để sản xuất acid nitric, một hợp chất hóa học quan trọng được sử dụng trong sản xuất thuốc nổ, sơn và chất tẩy rửa.
Ngoài ra, phản ứng S + HNO3 còn được sử dụng để sản xuất acid sulfamic, một hợp chất hữu ích trong các ứng dụng hóa học và công nghiệp, như là chất tẩy rửa, chất chống ô nhiễm, và chất làm mềm nước. Acid sulfamic còn được sử dụng để làm sạch bề mặt kim loại và xử lý nước.
Bài tập về axit nitric (HNO3) – Hóa học 11- Thầy Phạm Thanh Tùng – YouTube
Hướng dẫn thực hiện phản ứng S + HNO3
Để thực hiện phản ứng S + HNO3, cần chuẩn bị các vật liệu và thiết bị sau:
- 90% axit nitric (HNO3)
- 90% axit sulfuric (H2SO4)
- Lưu huỳnh (S)
- Bình kính (Erlenmeyer flask)
- Ống nghiệm (test tube)
- Bình đựng nước (water bath)
- Bộ lọc và bình thu mẫu (filter and sample vial)
- Găng tay bảo vệ
- Kính bảo vệ (safety goggles)
- Áo bảo hộ (lab coat)
Bước 1: Đeo đầy đủ trang bị bảo hộ gồm găng tay, kính bảo vệ và áo bảo hộ để đảm bảo an toàn cho quá trình thực hiện phản ứng.
Bước 2: Trộn lưu huỳnh với 90% axit nitric trong bình kính (Erlenmeyer flask) với tỷ lệ 1:4 (sulfuric acid:nitric acid). Đảm bảo lưu huỳnh tan hoàn toàn trong dung dịch axit nitric.
Bước 3: Đun nóng dung dịch trong bình kính bằng bình đựng nước (water bath) với nhiệt độ khoảng 120-130 độ C trong khoảng 30 phút. Quá trình đun nóng phải được thực hiện ở nơi thoáng khí và độc tốt.
Bước 4: Điều chỉnh nhiệt độ bình đựng nước để duy trì nhiệt độ khoảng 120-130 độ C trong suốt quá trình phản ứng.
Bước 5: Để quá trình phản ứng hoàn tất, dung dịch sẽ chuyển từ màu vàng sang màu nâu đỏ, và sẽ bắt đầu tỏa ra mùi khó chịu do NO2.
Bước 6: Cho dung dịch qua bộ lọc để tách bỏ kết tủa và chất lỏng còn lại được sử dụng trong các ứng dụng khác.
Chú ý an toàn khi thực hiện phản ứng S + HNO3
Việc thực hiện phản ứng S + HNO3 là một quá trình nguy hiểm vì có thể sinh ra các chất độc hại như NO2 và SO.
Vì vậy, để đảm bảo an toàn trong quá trình thực hiện, cần tuân thủ các quy định an toàn sau:
- Đeo đầy đủ trang bị bảo hộ gồm găng tay, kính bảo vệ và áo bảo hộ khi thực hiện phản ứng.
- Thực hiện phản ứng ở nơi thoáng khí và độc tốt, tránh tiếp xúc với khói, hơi độc hại và dung dịch phản ứng.
- Đảm bảo nhiệt độ và áp suất trong quá trình phản ứng được kiểm soát để tránh các tác động độc hại đến người thực hiện.
- Không được pha trộn dung dịch axit sulfuric và axit nitric khi chưa chuẩn bị sẵn đầy đủ trang bị bảo hộ và thiết bị cần thiết.
- Nếu xảy ra sự cố trong quá trình thực hiện phản ứng, cần ngay lập tức dừng lại, tắt nguồn nhiệt và thông báo cho cấp trên hoặc nhân viên y tế trong trường hợp cần thiết.
Ứng dụng của phản ứng S + HNO3
Phản ứng S + HNO3 được sử dụng trong nhiều ứng dụng khác nhau, bao gồm:
- Sản xuất thuốc nhuộm: Phản ứng S + HNO3 được sử dụng để sản xuất hơn 80% các loại thuốc nhuộm. Lưu huỳnh sau khi phản ứng sẽ được sử dụng để sản xuất một số loại thuốc nhuộm, ví dụ như acid sulfuric trong việc sản xuất thuốc nhuộm màu đen.
- Sản xuất phân bón: Lưu huỳnh sản xuất từ phản ứng S + HNO3 được sử dụng để sản xuất phân bón sulfat. Phân bón sulfat được sử dụng để cải tạo đất và cung cấp lưu huỳnh cho cây trồng.
- Sản xuất thuốc trừ sâu: Phản ứng S + HNO3 được sử dụng để sản xuất các hợp chất hữu cơ có chứa lưu huỳnh, nhưngylate và thiodicarb, được sử dụng như là các thành phần chính của một số loại thuốc trừ sâu.
Với nhiềuứng dụng quan trọng, phản ứng S + HNO3 đã đóng góp rất lớn cho nhiều ngành công nghiệp và đời sống của con người.
Sản xuất thuốc nhuộm
Trong ngành công nghiệp dệt may, thuốc nhuộm được sử dụng để tạo màu sắc cho các sản phẩm vải. Đối với sản xuất thuốc nhuộm màu đen, lưu huỳnh là một thành phần chính được sử dụng. Lưu huỳnh được sản xuất từ phản ứng S + HNO3. Sau khi phản ứng xảy ra, sản phẩm thu được là acid sulfuric và khí nitơ dioxide. Lưu huỳnh được chiết xuất từ acid sulfuric, sau đó được sử dụng để sản xuất thuốc nhuộm màu đen.
Sản xuất phân bón
Phân bón là một thành phần quan trọng trong nông nghiệp và sản xuất thực phẩm. Trong đó, lưu huỳnh là một nguyên tố dinh dưỡng cần thiết cho cây trồng. Phản ứng S + HNO3 được sử dụng để sản xuất lưu huỳnh. Sau khi phản ứng xảy ra, sản phẩm thu được là acid sulfuric và khí nitơ dioxide. Lưu huỳnh được chiết xuất từ acid sulfuric và sau đó được sử dụng để sản xuất phân bón sulfat. Phân bón sulfat cung cấp lưu huỳnh cho cây trồng và giúp cải tạo đất.
Sản xuất thuốc trừ sâu
Trong ngành nông nghiệp, việc kiểm soát sâu bệnh trên cây trồng là rất quan trọng để tăng năng suất và chất lượng sản phẩm. Thuốc trừ sâu là một công cụ hiệu quả trong việc kiểm soát sâu bệnh. Trong thuốc trừ sâu, hợp chất hữu cơ có chứa lưu huỳnh được sử dụng để giết sâu. Phản ứng S + HNO3 được sử dụng để sản xuất các hợp chất hữu cơ này. Sau khi phản ứng xảy ra, lưu huỳnh được chiết xuất và sau đó được sử dụng để sản xuất các hợp chất hữu cơ như thiodicarb và như butylate. Các hợp chất này được sử dụng như là thành phần chính trong thuốc trừ sâu để giết sâu và bảo vệ cây
Sản xuất thuốc tẩy
Thuốc tẩy là một trong những sản phẩm được sử dụng rộng rãi trong đời sống hàng ngày để làm sạch. Trong quá trình sản xuất thuốc tẩy, lưu huỳnh được sử dụng để tạo ra một số loại hóa chất. Phản ứng S + HNO3 được sử dụng để sản xuất lưu huỳnh. Sau khi phản ứng xảy ra, sản phẩm thu được là acid sulfuric và khí nitơ dioxide. Lưu huỳnh được chiết xuất từ acid sulfuric và sau đó được sử dụng để sản xuất một số loại hóa chất như sulfoxylate và sulfite. Các hợp chất này được sử dụng trong quá trình sản xuất thuốc tẩy để giúp tẩy sạch bụi bẩn và vết bẩn trên các bề mặt khác nhau.
Sản xuất pin
Pin là một nguồn năng lượng quan trọng trong đời sống hàng ngày. Pin được sử dụng trong nhiều thiết bị điện tử, từ điện thoại di động đến máy tính xách tay. Trong quá trình sản xuất pin, acid sulfuric được sử dụng để tạo ra một số loại pin khác nhau. Phản ứng S + HNO3 được sử dụng để sản xuất acid sulfuric. Sau khi phản ứng xảy ra, sản phẩm thu được là acid sulfuric và khí nitơ dioxide. Acid sulfuric được sử dụng để sản xuất pin acid chì và pin alkali chì. Các loại pin này được sử dụng trong các thiết bị điện tử khác nhau.
Tổng kết
Phản ứng S + HNO3 là một trong những phản ứng quan trọng trong hóa học vì nó tạo ra hai sản phẩm chính là H2SO4 và NO2. Cơ chế phản ứng là phức tạp, nhưng cách thức thực hiện phản ứng khá đơn giản. Tuy nhiên, việc thực hiện phản ứng này cần phải được thực hiện rất cẩn thận, vì nó có thể tạo ra một số chất độc hại, như NO2 và SO2. Phản ứng S + HNO3 được sử dụng rộng rãi trong sản xuất phân bón, hóa chất công nghiệp và các sản phẩm hữu ích khác trong cuộc sống hàng ngày.
Bạn Đang Xem Bài Viết: Quá trình phản ứng S + HNO3? Hướng dẫn và ứng dụng”







































